1. Contesto normativo
Da Gennaio 2024 le farmacie dovranno registrare elettronicamente i dati relativi ad alcune categorie di medical device e diagnostici in vitro. Nello specifico tale obbligo di registrazione e conservazione in modalità elettronica partirà dall’8 Gennaio 2024 per i diagnostici in vitro e dal 15 Gennaio 2024 per quanto riguarda i medical device.
La mancata osservanza di tali obblighi normativi è punita con ammenda da € 4.000 a € 24.500.Il DM 11 maggio 2023 prevede che le Istituzioni e gli Operatori del settore sanitario conservino i codici UDI di alcune categorie di dispositivi medici, in particolare per le farmacie:
- dispositivi di classe III impiantabili (ad es. spirali intrauterine) -> registrare e conservare i codici UDI delle confezioni ricevute e fornite;
- dispositivi di classe III, diversi dai dispositivi impiantabili (ad es. siringhe interarticolari, intradermiche, spirali intrauterine); dispositivi impiantabili di classe IIb (ad es. alcune fiale per siringhe intra-articolari) ad eccezione dei dispositivi usati in odontoiatria e di materiale per sutura -> registrare i codici UDI delle confezioni ricevute;
- diagnostici in vitro appartenenti alla classe D (ad es. test per rilevazione epatite) -> registrare i codici UDI delle confezioni ricevute.
Si precisa che gli obblighi di registrazione – non espressamente riferiti ai codici UDI dei dispositivi ricevuti/forniti prima dei termini previsti – riguardano i dispositivi ricevuti/forniti a partire dall’8 Gennaio 2024 (diagnostici in vitro) o dal 15 Gennaio 2024 (medical device) ed interessano anche i dispositivi destinati alla vendita online.
Le farmacie, dietro specifica richiesta, dovranno ricevere dagli operatori economici, al momento dell’acquisto, tutte le informazioni necessarie ai loro obblighi di registrazione e conservazione. Le informazioni registrate dovranno essere conservate per un periodo minimo di 10 anni a partire dalla data di registrazione.
2. Operazioni propedeutiche di registrazione utente
Grazie al supporto tecnico di Farmadati è stata creata una repository personalizzata dove ogni farmacia potrà registrare e conservare tutti i dati relativi ai dispositivi, acquistati dalla farmacia, che necessitano di tale registrazione.
Al fine di poter procedere la farmacia dovrà registrarsi al portale web dedicato:
- collegarsi al link https://dm.farmadati.it/
- cliccare la voce “Registrati” in basso a destra;
- compilare i campi richiesti dal modulo di registrazione (i campi obbligatori sono contrassegnati con asterisco);
- spuntare la casella “ho preso visione dell’informativa dettagliata sulla Privacy”;
- cliccare “REGISTRATI” in basso al centro (bottone verde): la mail con le credenziali sarà inviata all’indirizzo e-mail inserito nel modulo di registrazione.
Fatto ciò sarà possibile accedere alla sezione “CODICI UDI REGISTRAZIONE CONSERVAZIONE” ed inserire:
- codice UDI, rilevabile anche da lettura ottica (stampato sulla confezione e che comprende UDI-DI + UDI-PI);
- data del movimento, selezionabile dal menu se diversa dalla data di sistema automaticamente impostata;
- tipo movimento, da menu a tendina: acquisizione o cessione.
3. Fasi operative da gestionale
Il gestionale, a partire dalla versione 3.0.4.94, consentirà a farmacisti ed operatori della farmacia di poter adempiere alla normativa vigente.
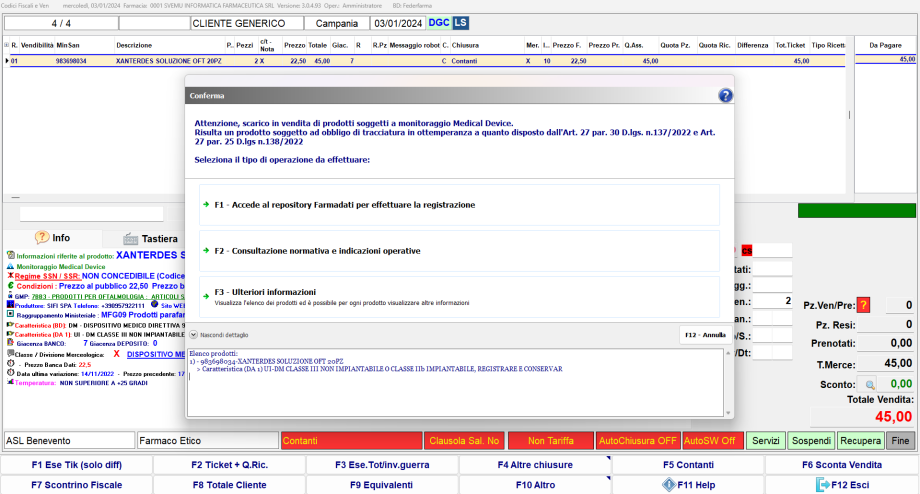
Più precisamente nella fase di carico prodotti (anche in evasione a stralcio) e di erogazione (vendita) dei prodotti interessati, sarà consentito con il tasto F1 collegarsi al portale web di Farmadati Italia per registrarsi e per poi provvedere alle operazioni di conservazione dei codici UDI o con i tasti F2 / F3 richiedere ulteriori informazioni a riguardo:
Dopo essersi registrati, in fase di successivo accesso al portale web per la conservazione dei codici UDI, sarà possibile inserire ovvero memorizzare nel gestionale le credenziali di accesso a Farmadati.
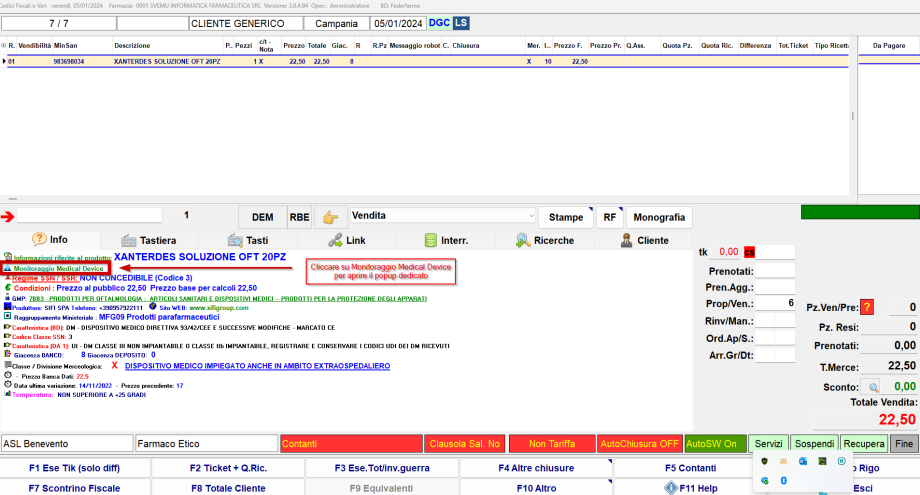
N.B. Il popup su riportato è riapribile anche in vendita, ovvero in fase di consultazione prodotti:

Lascia un commento: